DIAGNÓSTICO MOLECULAR DA INFERTILIDADE
Infertilidade Masculina e Feminina
A fertilidade é a capacidade natural de um indivíduo ou casal de conceber e produzir descendência. Esta capacidade depende de vários fatores biológicos, relacionados tanto à saúde reprodutiva masculina quanto feminina.
Já a infertilidade é a incapacidade de conceber após um ano de tentativas regulares de gravidez sem o uso de contraceptivos.
Segundo a Organização Mundial de Saúde (OMS), a infertilidade afeta cerca de 186 milhões de indivíduos no mundo, dos quais 20-30% são causados por fatores masculinos, 20-35% por fatores femininos e o restante são fatores do casal. No Brasil, aproximadamente 8 milhões de indivíduos não conseguem ter filhos.
A infertilidade possui múltiplas causas. Infecções sexualmente transmissíveis, alterações cromossômicas e a presença de mutações no DNA associadas à fibrose cística podem causar infertilidade em homens e mulheres. Em relação a infertilidade feminina, podemos destacar a endometrite crônica (EC), as trombofilias e a síndrome do X frágil. Já entre as causas de infertilidade masculina, destacamos as microdeleções no cromossomo Y.
Infecções Sexualmente Transmissíveis (IST)
As infecções sexualmente transmissíveis (IST), são causadas por vírus, bactérias, fungos e protozoários, e transmitidas por meio de contato sexual com indivíduos infectados, sem uso de preservativo. Essas doenças podem se manifestar através de bolhas, verrugas, feridas e corrimentos, ou podem não apresentar sintomas. Quando não tratadas, podem trazer danos permanentes tanto no trato reprodutor feminino quanto no masculino, podendo acarretar complicações graves, como a infertilidade.
ISTs e infertilidade feminina
A saúde reprodutiva feminina é fortemente influenciada pela microbiota vaginal. A vaginose bacteriana, causada pela Gardnerella vaginalis, e a inflamação do trato genital superior, doença inflamatória pélvica (DIP), causada por outros patógenos, como a Chlamydia trachomatis e a Neisseria gonorrhoeae, são importantes fatores causadores de infertilidade e problemas na gestação, como partos prematuros, abortos espontâneos, gravidez ectópica, infertilidade tubária e infecção materno-fetal.
Portanto, é fundamental o diagnóstico e tratamento adequados para prevenir a infertilidade e outras complicações relacionadas a essas infecções.
Exames disponíveis para diagnóstico de ISTs
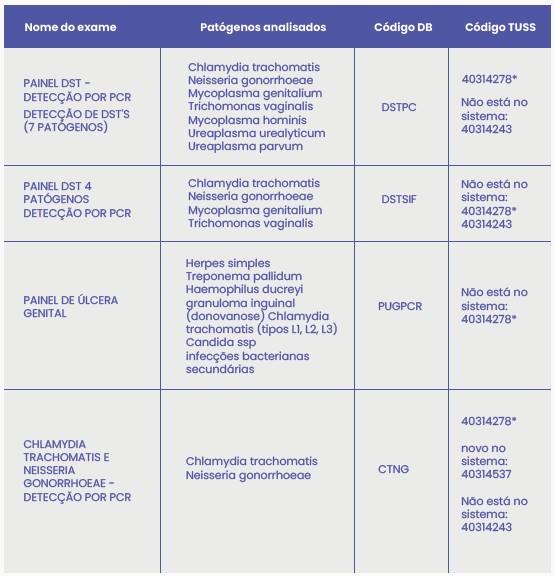
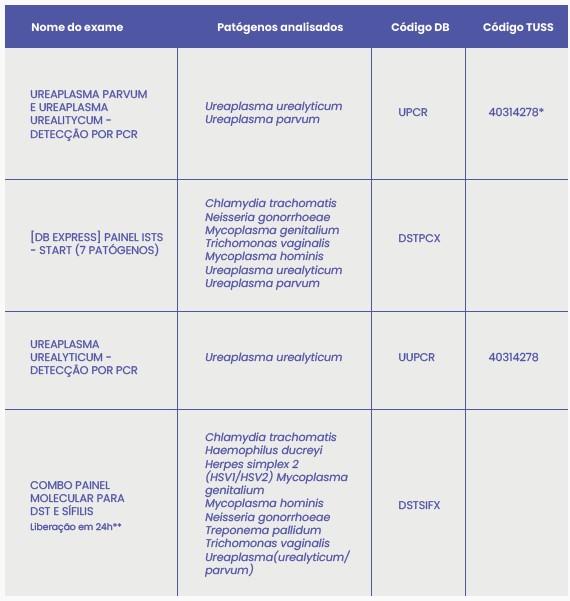
* Código TUSS genérico para detecção de agentes infecciosos por PCR. Verifique com o convênio referente à aceitação do uso desse código.
**DB Express: DSPTCX e DSTSIFX: resultados em até 24h após a chegada da amostra no laboratório. Consulte com seu representante a disponibilidade desses exames na sua região.
Caso necessário, também realizamos a pesquisa dos patógenos de forma isolada.
Qualquer dúvida, acesse nosso Guia de Exames.
Anormalidades cromossômicas
Anormalidades cromossômicas são importantes causas de infertilidade em homens e mulheres, influenciando tanto a qualidade dos óvulos e espermatozoides quanto o desenvolvimento embrionário. Estima-se que alterações cromossômicas, tanto numéricas quanto estruturais, sejam responsáveis por 2 a 14% da infertilidade masculina e até 10% da infertilidade feminina. Além disso, anormalidades cromossômicas no feto, como as aneuploidias, onde há um número anormal de cromossomos, são causas comuns de abortos espontâneos e falhas no desenvolvimento.
Exames disponíveis para detecção de anormalidades cromossômicas
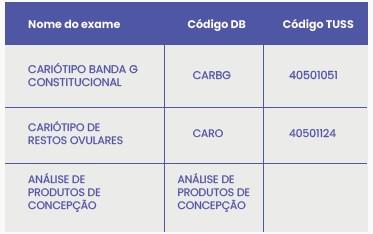
Fibrose cística
A Fibrose Cística, conhecida também como Doença do Beijo Salgado ou Mucoviscidose, é uma doença autossômica recessiva causada por mutações no gene Regulador da Condutância Transmembrana em Fibrose Cística (CFTR). Mutações no CFTR alteram o transporte de íons cloro e sódio através das membranas celulares, o que leva ao acúmulo de muco espesso e pegajoso nos pulmões, pâncreas e outros órgãos, afetando suas funções.
A fibrose cística pode afetar a fertilidade tanto em homens quanto em mulheres, embora seja mais comumente associada à infertilidade masculina. Nos homens, a doença frequentemente causa obstrução do ducto deferente, um fenômeno conhecido como azoospermia obstrutiva, decorrente da ausência congênita bilateral do ducto deferente (CBAVD). Este problema impede a passagem dos espermatozoides, levando à infertilidade na maioria dos casos, apesar de os homens continuarem a produzir espermatozoides . Nas mulheres, embora seja menos comum, a fibrose cística pode impactar a fertilidade devido ao espessamento do muco cervical, que dificulta a passagem dos espermatozoides.
Exames disponíveis para detecção de Fibrose cística
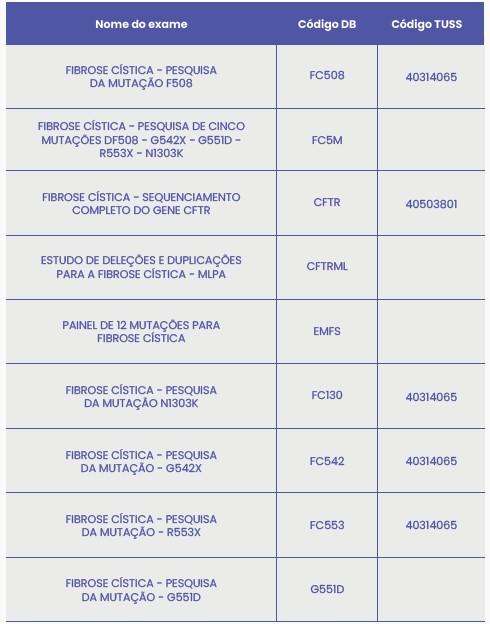
Infertilidade masculina
Microdeleções no cromossomo Y
O cromossomo Y desempenha um papel essencial na determinação do sexo masculino, sendo fundamental no desenvolvimento dos testículos e na espermatogênese. Este cromossomo contém uma região crítica conhecida como AZF (Azoospermia Factor), subdividida em três partes: AZFa, AZFb, e AZFc, localizadas no braço longo do cromossomo. Estas regiões são vitais para a produção de espermatozoides, e microdeleções nelas podem resultar em condições variando de oligozoospermia (baixa contagem de espermatozoides) a azoospermia (ausência de espermatozoides), ambas associadas à infertilidade masculina. Pesquisas indicam que até 10% dos homens com infertilidade severa apresentam microdeleções na região AZFc do cromossomo Y.
Além disso, o gene SRY, localizado no braço curto do cromossomo Y, é essencial para o desenvolvimento testicular. As mutações ou ausência do gene SRY podem impedir o desenvolvimento normal dos testículos, resultando em condições que afetam a identidade sexual e reprodutiva dos indivíduos afetados.
Para diagnosticar microdeleções no cromossomo Y, utilizam-se testes específicos que investigam a presença de sequências de DNA específicas (STS - Sequence-tagged Sites) dentro das regiões AZF, além de técnicas como análise de microarranjos cromossômicos e hibridização fluorescente in situ (FISH), capazes de identificar as microdeleções nas
áreas AZFa, AZFb, e AZFc.
A prevalência significativa de microdeleções no cromossomo Y entre homens inférteis ressalta a importância de uma avaliação genética detalhada nesses casos, abrindo caminho para intervenções mais precisas e tratamentos eficazes, oferecendo esperança para muitos casais enfrentando desafios na reprodução.
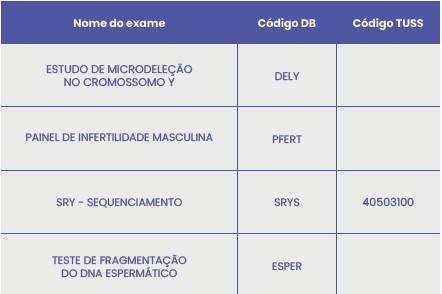
Exames disponíveis para detecção de microdeleções no cromossomo Y
Infertilidade Feminina
Endometrite crônica
A endometrite crônica é caracterizada por uma inflamação persistente do endométrio, comumente diagnosticada por meio de exames histopatológicos, que identificam a presença anormal de plasmócitos. Métodos complementares, como a histeroscopia e análises de microbioma, também são utilizados para detecção de patógenos específicos. Testes genéticos, como PCR em tempo real e o Sequenciamento de Nova Geração (NGS), são empregados para quantificar DNA bacteriano, auxiliando na identificação precisa dos agentes causadores e na orientação do tratamento. Essa abordagem multidisciplinar é essencial para tratar a condição e mitigar seus efeitos sobre a fertilidade.
As bactérias mais comumente analisadas no diagnóstico de endometrite crônica são:
• Enterococcus spp.
• Streptococcus spp.
• Staphylococcus spp.
• Enterobacteria (e.g. Escherichia coli, Klebsiella pneumoniae)
• Mycoplasma spp.
• Ureaplasma spp.
• Chlamydia trachomatis
• Neisseria gonorrhoeae
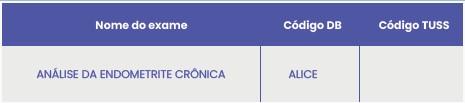
Exames disponíveis para diagnóstico de endometrite crônica
Trombofilia
A trombofilia é uma condição genética caracterizada pela predisposição ao desenvolvimento de trombose devido a anomalias no sistema de coagulação e está presente em uma proporção significativa de casos de perda gestacional recorrente. A hipercoagulabilidade está associada a abortos de repetição e à falha da implantação do embrião no útero.
Algumas mutações associadas à trombofilia, como a mutação no gene da protrombina (G20210A) e a mutação no fator V de Leiden (R506Q), constituem importantes fatores de risco para o desenvolvimento de tromboembolismo venoso e a formação de coágulos durante a gestação. A mutação no fator V de Leiden em heterozigose está associada a um risco duas a três vezes maior de perda fetal, além de possivelmente outras complicações da gravidez, como pré-eclâmpsia/eclâmpsia, alteração no crescimento fetal e descolamento de placenta.
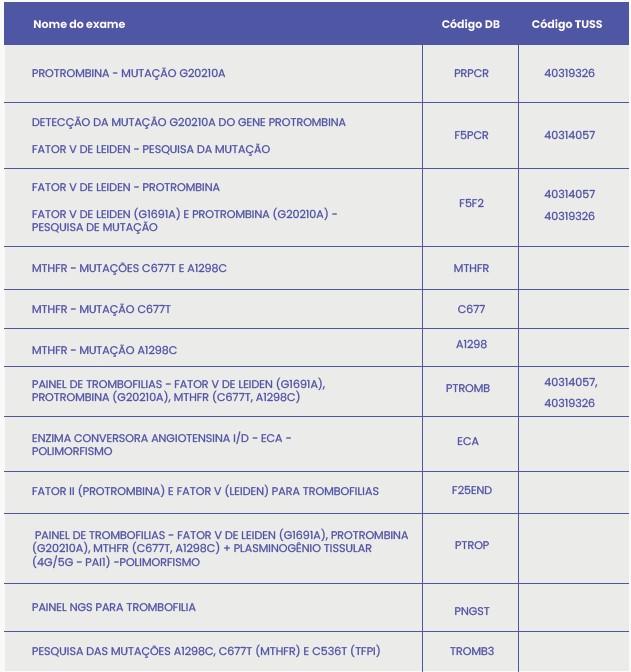
Exames disponíveis para diagnóstico de trombofilia
Síndrome do X frágil
A Síndrome do X Frágil é causada por uma mutação no gene FMR1, que resulta no alongamento de uma sequência de CGG no cromossomo X. Quando essa sequência excede 200 repetições, ocorre a inibição da produção normal da proteína FMRP, essencial para o desenvolvimento neurológico, resultando nos sintomas característicos da síndrome. Mulheres portadoras de pré-mutações, com repetições de 55 a 200 CGG, têm um risco aumentado de desenvolver insuficiência ovariana primária associada ao X frágil (FXPOI), que é uma causa significativa de disfunção ovariana.
A prevalência de FXPOI em mulheres com pré-mutação varia, mas estudos sugerem que cerca de 20% dessas mulheres desenvolvem insuficiência ovariana primária ao longo de sua vida reprodutiva, uma taxa significativamente maior do que a observada na população geral, que é de aproximadamente 1%.
A análise genética do gene FMR1 permite identificar a presença de pré-mutações e estimar o risco de desenvolvimento de condições associadas, como FXPOI . A determinação precisa do número de repetições CGG é primordial para o diagnóstico correto e o aconselhamento genético apropriado.
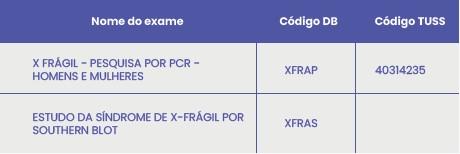
Exames disponíveis para diagnóstico da síndrome do X frágil
Alterações no sistema imunológico
O sistema imunológico participa ativamente do processo de fertilização. Por meio dele, ocorre uma série de mecanismos que contribuem para o curso normal da gestação. Por isso, disfunções nas células imunológicas estão relacionadas às causas de infertilidade feminina.
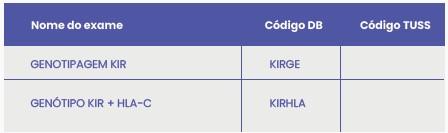
Exames disponíveis para diagnóstico de alterações imunológicas
Diagnóstico de infertilidade feminina por imuno-histoquímica
A imuno-histoquímica é uma técnica significativa no diagnóstico de infertilidade feminina, especialmente para identificar condições subclínicas que impactam a fertilidade, como a endometrite crônica e a endometriose. Ela permite a detecção específica de células inflamatórias e outros marcadores no tecido endometrial, oferecendo uma abordagem mais precisa para identificar patologias que podem não ser evidentes em exames padrão. Isso facilita um diagnóstico mais acurado e a implementação de tratamentos específicos, potencialmente melhorando as taxas de sucesso da concepção em mulheres com dificuldades de engravidar.diagnóstico correto e o aconselhamento genético apropriado.
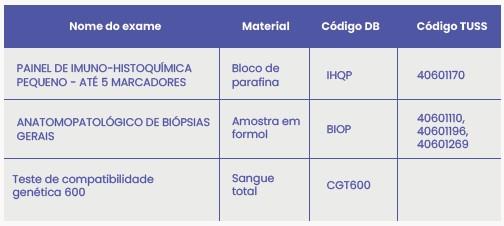
Exames de imuno-histoquímica disponíveis para diagnóstico de infertilidade feminina
Indicações
• Casais que estão com dificuldades de conceber
• Mulheres que experimentaram falhas de implantação ou abortos recorrentes
• Mulheres com reserva ovariana diminuída ou falência ovariana prematura
• Mulheres com ciclos menstruais irregulares, amenorreia ou problemas de ovulação
• Casais com histórico de doenças genéticas na família
• Homens com oligospermia ou azoospermia
Como solicitar?
Escrever na solicitação médica o nome do patógeno, gene ou doença que se deseja investigar seguido pela metodologia desejada. Se possível, usar o código DB do exame.
Exemplo 1: Pesquisa de X frágil por PCR (XFRAP)
Exemplo 2: Pesquisa gene MTHFR mutação A1298C por PCR (A1298)
Referências
https://pubmed.ncbi.nlm.nih.gov/33603438/ Rabinowitz MJ, Huffman PJ, Haney NM, Kohn TP. Y-Chromosome Microdeletions: A Review of Prevalence, Screening, and Clinical
Considerations. Appl Clin Genet. 2021;14:51-59. Published 2021 Feb 12. doi:10.2147/TACG.S267421
Fan Y, Silber SJ. Y Chromosome Infertility. 2002 Oct 31 [Updated 2019 Aug 1]. In: Adam MP, Feldman J, Mirzaa GM, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2024. Available from: https://www.ncbi.nlm.nih.gov/books/NBK1339/
Ahmad A, Ahmed A, Patrizio P. Cystic fibrosis and fertility. Curr Opin Obstet Gynecol. 2013;25(3):167-172. doi:10.1097/GCO.0b013e32835f1745
Castro, J., Machado, D. & Cerca, N. Unveiling the role of Gardnerella vaginalis in polymicrobial Bacterial Vaginosis biofilms: the impact of other vaginal pathogens living as
neighbors. ISME J 13, 1306–1317 (2019). https://doi.org/10.1038/s41396-018-0337-0
Kairys N, Carlson K, Garg M. Gardnerella Vaginalis. [Updated 2023 Nov 12]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan-. Available from:
https://www.ncbi.nlm.nih.gov/books/NBK459350/
https://www.cff.org/managing-cf/fertility-women-cf
Yasuo T, Kitaya K. Challenges in Clinical Diagnosis and Management of Chronic Endometritis. Diagnostics. 2022; 12(11):2711. https://doi.org/10.3390/diagnostics12112711
Liu X, Chen Y, Ye C, et al. Hereditary thrombophilia and recurrent pregnancy loss: a systematic review and meta-analysis. Hum Reprod. 2021;36(5):1213-1229.
doi:10.1093/humrep/deab010
Hamedi B, Feulefack J, Khan A, Sergi C. Association between factor V Leiden mutation and recurrent pregnancy loss in the middle east countries: a Newcastle-Ottawa
meta-analysis. Arch Gynecol Obstet. 2020;302(2):345-354. doi:10.1007/s00404-020-05610-6
https://www.nichd.nih.gov/health/topics/fxpoi/conditioninfo
https://fragilex.org/understanding-fragile-x/fxpoi-primary-ovarian-insufficiency/
https://www.frontiersin.org/articles/10.3389/fnmol.2017.00290/full
Hunter JE, Berry-Kravis E, Hipp H, et al. FMR1 Disorders. 1998 Jun 16 [Updated 2019 Nov 21]. In: Adam MP, Feldman J, Mirzaa GM, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993-2024. Available from: https://www.ncbi.nlm.nih.gov/books/NBK1384/




